Kamis, 01 November 2012
Minggu, 28 Oktober 2012
Spektroskopi dengan sinar ultraviolet (UV) dan sinar tampak (VIS)
Spektroskopi dengan sinar ultraviolet (UV) dan sinar tampak (VIS) à Metoda ini sangat sensitif dan dengan demikian sangat cocok untuk tujuan analisis. Lebih lanjut,spetroskopi UV-VIS sangat kuantitatif dan jumlah sinar yang diserap oleh sampel diberikan oleh ungkapan hukum Lambert-Beer. Menurut hukum ini, absorbans larutan sampel sebanding dengan panjang lintasan cahaya d dan konsentrasi larutannya c. Umumnya spektroskopi dengan sinar ultraviolet (UV) dan sinar tampak (VIS) dibahas bersama karena sering kedua pengukuran dilakukan pada waktu yang sama.
spektroskopik infra merah
Spektroskopi infra merah (IR) à Metode spektroskopi inframerah merupakan suatu metode yang meliputi teknik serapan (absorption), teknik emisi (emission), teknik fluoresensi (fluorescence). Metode Spektroskopi inframerah ini dapat digunakan untuk mengidentifikasi suatu senyawa yang belum diketahui, karena spektrum yang dihasilkan spesifik untuk senyawa tersebut.
Metode spektroskopik
Spektroskopis adalah ilmu yang mempelajari materi dan atributnya berdasarkan cahaya, suara atau partikel yang dipancarkan, diserap atau dipantulkan oleh materi. Sebagai ilmu yang mempelajari interaksi antara cahaya dan materi. Alat untuk merekam spektrum disebut spectrometer.
Potensial sel
Potensiual sel volta dapat ditentukan melalui percobaan dengan menggunakan potensiometer,
Potensial sel sama dengan jumlah potensial standar elektrodanya.
Potensial sel sama dengan jumlah potensial standar elektrodanya.
Berbagai kristal
1.Kristal logam terbentuk atas atom logam yang terikat dengan ikatan logam
2.Kristal ionik dibentuk oleh gaya tarik antara ion yang bermuatan positif dan negatif
3.Kristal molekular terikat oleh gaya antar molekul disebut kristal molekular
2.Kristal ionik dibentuk oleh gaya tarik antara ion yang bermuatan positif dan negatif
3.Kristal molekular terikat oleh gaya antar molekul disebut kristal molekular
Larutan
Larutan adalah fasa cair yang berupa sistem dua atau multi componen
Larutan terdiri atas cairan yang melarutkan dan zat yang larut didalamnnya (zat terlarut)
Zat terlarut dapat berwujud padat,cair dan gas.
Larutan terdiri atas cairan yang melarutkan dan zat yang larut didalamnnya (zat terlarut)
Zat terlarut dapat berwujud padat,cair dan gas.
materi netralisai
Netralisasi adalah reaksi antara ion hodronium dan ion hidroksida yang membentuk air
Kurva titrasi adalah kurva yang menunjukan grafik volume penitar pada sumbu x
Kurva titrasi adalah kurva yang menunjukan grafik volume penitar pada sumbu x
Senin, 22 Oktober 2012
diagram fasa
Diagram fasaDiagram fasa adalah suatu grafik yang merupakan representasi tentang fasa-fasa yang ada dalam suatu material pada variasi temperatur, tekanan dan komposisi.Dalam kimia fisik, mineralogi, dan teknik material, diagram fase adalah sejenisgrafik yang digunakan untuk menunjukkan kondisi kesetimbangan antara fase-faseyang berbeda dari suatu zat yang sama. Dalam matematika dan fisika, diagram fase juga mempunyai arti sinonim dengan ruang fase.
kesetimbangan fasa
KESETIMBANGAN FASA
Bagian sesuatu yang menjadi pusat perhatian dan dipelajari disebut sebagai
sistem. Suatu sistem heterogen terdiri dari berbagai bagian yang homogen yang saling
bersentuhan dengan batas yang jelas. Bagian homogen ini disebut sebagai fasa dapat
dipisahkan secara mekanik.
Tekanan dan temperatur menentukan keadaan suatu materi kesetimbangan fasa
dari materi yang sama. Kesetimbangan fasa dari suatu sistem harus memenuhi syarat
berikut :
a. Sistem mempunyai lebih dari satu fasa meskipun materinya
sama
b. Terjadi perpindahan reversibel spesi kimia dari satu
fasa ke fasa lain
c. Seluruh bagian sistem mempunyai tekanan dan temperatur
sama
Kesetimbangan fasa dikelompokan menurut jumlah komponen penyusunnya
yaitu sistem satu komponen, dua komponen dan tiga komponen Pemahaman mengenai
perilaku fasa berkembang dengan adanya aturan fasa Gibbs. Sedangkan persamaan
Clausius dan persamaan Clausius Clayperon menghubungkan perubahan tekanan
kesetimbangan dan perubahan suhu pada sistem satu komponen. Adanya penyimpangan
dari sistem dua komponen cair- cair ideal konsep sifat koligatif larutan dapat
dijelaskan
Minggu, 07 Oktober 2012
Kesimpulan jurnal pengolahan limbah
Limbah B3 menurut jenisnya terdiri dari limbah tidak spesifik,sumber spesifik,dan bahan kimia kadaluarsa
dan nilai akhir dari limbah yakni dosis/konsentrasi bahan uji menimbulkan kematian 50% hewan uji
dan nilai akhir dari limbah yakni dosis/konsentrasi bahan uji menimbulkan kematian 50% hewan uji
Sabtu, 06 Oktober 2012
Sabtu, 29 September 2012
Sabtu, 22 September 2012
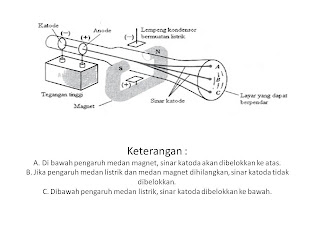
penemuan elektron dalam sebuah percobaan sinar katoda
BAGAIMANA AWAL MULA ELEKTRON DITEMUKAN?
Ternyata untuk menemukan sebuah elektron para ilmuan perlu melakukan percobaan yang dilakukan salah satunya adalah dengan cara mempelajari hamparan listrik dalam tabung hampa.
Percobaan yang dilakukan adalah dengan cara tabung kaca yang dilengkapi dengan dua keping logam
yang bertindak sebagai elektrodanya dimana elektroda
yang positif disebut anoda dan elektroda nehatif disebut katoda,kemudian kedalam tabung dimasukan gas
yang tekanannya sangat rendah
(0,01 mm hg) dan dihubungkan dengan listrik yang tegangannya sangat tinggi(>1000
volt) kemudian terjadilah pancaran sinar
yang diduga berasal dari katoda menuju anoda,dan dapat disimpulkan sinar tersebut dinamakan dengan sinar katoda.
penemuan elektron
Kesimpulan yang dapat diambil adalah elekrtro pasti
bermuatan negative terletak dalam atom dan menyebabkan sifat kimia
lahirnya mekanika kuantum
Kesimpulan yang dapat diambil adalahTeori mekanika kuantum mengemukakan bahwa posisi electron
tidak dapat ditentukan.
ikatan jenis kimia
Kesimpulan yang dapat diambil adalah
Ikatan kimia terbagi menjadi 2 jenis yaitu ikatan jenis atom
dan ikatan jenis molekul
Ikatan ion = heteropolar
Ikatan kovalen =homopolar
Ikatan kovalen koordinasi =semipolar
sejarah lahirnya kimia
Kesimpulannya adalah kimia terlahir berawal dari
ditemukannya oksigen secara independen oleh dua kimiawan asal inggris dan
swedia.kimia modern terlahir oleh
kimiawan perancis yang dapat menge,bangkan peran oksigen dalam pembakaran
menjadi sebuah hokum kekekalan massa dalam reaksi kimia.
struktur senyawa anorganik
Kesimpulan yang dapat diambil adalahBasa dapat menghasilkan ion logam yang bermuatan positif
serta gugus hidroksil (oh-)yang bermuatan negative.
Asam adalah dapat menghasilkan ion h+ dan ion sisa asam yang
bermuatan negative
Garam/netral dapat terbentuk dari asam bila semua atom h
diganti dengan logam,terbentuk dari basa bila semua gugus OH diganti dengan
sisa asam.
kimia modern
yang dapat saya rangkum dari materi kelompok ini adalah Kimia modern dimulai oleh kimiawan perancis Antoine Laurent
Lavoisier (1743-1794).ia menemukan hokum kekekalan massa dalam reaksi kimia dan
mengungkap peran oksigen dalam pembakaran.
dasar dasar teori kuantum klasik
Kesimpulan yang dapat diambil adalah dasar dasar teori kuantum klasik dibagi menjadi dua:
a.spektrum atom
b.model bohr
salah satu teori bohr adalah tidak ada energy yag
dipancarkan bila electron berada electron dalam atom
c. spekta atom hydrogen
d.hukum Moseley
e.keterbatasan teori bohr
model atom
yang dapat saya simpulkan dari materi ini adalah
a.ukuran atom
karena atom adalah benda konkrit atau benda nyata
pendekatan volume atom =volume 1 mol padatan/konstanta
avrogado
model atom mendefinisikan bahwa model atom berupa roti
kismis
b.penemuan inti atom
penemuan inti atom
dilakukan percobaan oleh ernest Rutherford (1871-1937) seorang fisikawan
inggris
kesimpulan dr percobaan bahwa muatan positif
atom terpusat dibgian pusat.
latihan struktur atom
yang dapat saya rangkum dari materi ini adalah
Proton bermuatan positif
Proton bermuatan positif
Electron bermuatan negative
Neutron bermuatan netral
Mencari neutron adalah masa dikurangi atom
Konfigurasi electron menunjukan jumlah kulit atom terluar.
Kamis, 20 September 2012
latihan struktur atom
karena saya belum banyak mengerti tentang latihan soal ini,saya akan memberikan satu buah contoh soal dan penjelasannya,
Latihan 2.8 Ketidakpastian posisi elektron.
Anggap anda ingin menentukan posisi elektron sampai nilai sekitar 5 x 10-12 m. Perkirakan ketidakpastian kecepatan pada kondisi ini.
Jawab: Ketidakpastian momentum diperkirakan dengan persamaan (2.13). p = h/
p = h/ x = 6,626 x 10-34 (J s)/5 x 10-12 (m) = 1,33 x 10-22 (J s m-1). Karena massa elektron 9,1065 x 10-31 kg, ketidakpastian kecepatannya
x = 6,626 x 10-34 (J s)/5 x 10-12 (m) = 1,33 x 10-22 (J s m-1). Karena massa elektron 9,1065 x 10-31 kg, ketidakpastian kecepatannya  v akan benilai:
v akan benilai:  v = 1,33 x 10-22(J s m-1) / 9,10938 x 10-31 (kg) = 1,46 x 108 (m s-1).
v = 1,33 x 10-22(J s m-1) / 9,10938 x 10-31 (kg) = 1,46 x 108 (m s-1).
Perkiraan ketidakpastian kecepatannya hampir setengah kecepatan cahaya (2,998 x108 m s-1) mengindikasikan bahwa jelas tidak mungkin menentukan dengan tepat posisi elektron. Jadi menggambarkan orbit melingkar untuk elektron jelas tidak mungkin.
sumber :http://www.file-edu.com/2011/11/materi-definisi-mekanika-kuantum.html
Latihan 2.8 Ketidakpastian posisi elektron.
Anggap anda ingin menentukan posisi elektron sampai nilai sekitar 5 x 10-12 m. Perkirakan ketidakpastian kecepatan pada kondisi ini.
Jawab: Ketidakpastian momentum diperkirakan dengan persamaan (2.13).
Perkiraan ketidakpastian kecepatannya hampir setengah kecepatan cahaya (2,998 x108 m s-1) mengindikasikan bahwa jelas tidak mungkin menentukan dengan tepat posisi elektron. Jadi menggambarkan orbit melingkar untuk elektron jelas tidak mungkin.
sumber :http://www.file-edu.com/2011/11/materi-definisi-mekanika-kuantum.html
Langganan:
Komentar (Atom)